
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
CLINICAL STUDIES / ETUDES CLINIQUES
IMAGERIE DES FISTULES ARTERIO-VEINEUSES DURALES A DRAINAGE VEINEUX PERI -MEDULLAIRE
IMAGING OF SPINAL DURAL ARTERIOVENOUS FISTULAS
E-Mail Contact - MELHAOUI Adyl :
adymelh@yahoo.com
RESUME Les fistules durales rachidiennes à drainage veineux périmédullaire constituent une pathologie d’individualisation récente. C’est les plus fréquentes des malformations vasculaires vertébromédullaires, elles se présentent sous la forme d’une myélopathie spastique progressive chez un sujet de plus de 40 ans. A partir d’une étude rétrospective des données cliniques et explorations radiologiques d’une série de 11 cas en IRM et artériographie médullaire, nous avons recensé l’ensemble des signes radiologiques qui orientent le diagnostic. L’IRM a montré un hypersignal T2 centromédullaire de façon constante ainsi que des vaisseaux périmédullaires pathologiques. L’angiographie médullaire reste l’examen clé pour le diagnostic. Elle a permit de montrer dans dix cas le shunt artério-veineux ainsi que ses afférences artériels et son retour veineux, permettant de planifier le traitement. Huit patients ont été pris en charge chirurgicalement avec exclusion de la fistule suivie d’une amélioration clinique. L’imagerie joue aussi un rôle important dans le suivi post-thérapeutique. L’IRM permet de mettre en évidence la disparition progressive des anomalies initiales, signe de l’efficacité du traitement. Mots clés : Fistule durale, Rachis, IRM, Angiographie ABSTRACT Spinal dural arteiovenous fistulas are the most frequent type of spinal vascular malformations. Usual clinical presentation is of progressive myelopathy in an adult above the age of 40 years. Based on a retrospective study of clinical and radiologic data (MRI and Angiography) concerning a series of 11 cases, we have collected all the radiologic finding that led to the diagnosis. In all cases MRI showed spinal cord abnormalities, consistent in a central T2 hypersignal and perimedullary flow voids. The angiography remains the gold standard method for diagnosis. It can show the exact location of the shunt unless it is thrombosed, as in one of our patients, thus allowing accurate treatment planning. Eight patients underwent a surgical treatment allowing the closure of the fistula that resulted in significant neurological improvement. Postoperative MRI shows the results of the treatment. The disappearance of preoperative abnormalities is a good indicator for the efficiency of the treatment. Spinal dural arteriovenous fistulas is still an underdiagnosed condition, the good knowledge of these typical imaging findings is mandatory for an early diagnosis and treatment. Key words : Dural fistula, Spine, MRI, Angiography INTRODUCTION Individualisées par KENDALL et LOGUE en 1977 (13) puis par MERLAND et coll en 1980 (18), les fistules durales rachidiennes à drainage veineux périmédullaires (FAVDPM) sont les plus fréquentes des anomalies artério-veineuses intra-rachidiennes. Elles sont rares et souvent méconnues, elles surviennent de façon prédominante chez l’homme de quarante à soixante ans et entraînent l’apparition d’une myélopathie chronique par hyperpression veineuse. En l’absence de traitement, l’évolution se fait lentement vers une paraplégie définitive. En nous appuyant sur l’étude de 11 observations cliniques et sur une revue de la littérature nous proposons une mise au point sur l’ensemble des anomalies radiologiques permettant d’évoquer le diagnostique, nous évaluerons également la place de l’imagerie dans le traitement et le suivi post thérapeutique de ces patients. MATERIEL ET METHODES Il s’agit d’une étude rétrospective des données cliniques et radiologique de 11 cas de fistules durales rachidiennes à drainage veineux péri-médullaires, explorées au service de neuroradiologie de l’hôpital des spécialités O.N.O de Rabat entre 1997 et 2002. Tous les patients ont bénéficié d’une IRM avec des séquences multiplanairesT1, T2 et T1 avec injection de gadolinium ainsi que d’une angiographie médullaire. Une Myélographie a été réalisée dans 1 cas. Le traitement à été chirurgical dans 8 cas. Deux patients ont refusé une prise en charge chirurgicale. Une embolisation a été réalisée dans un cas. RESULTATS Nos observations portent sur onze cas de FAVDPM colligées entre 1997 et 2002 sur un ensemble de 16 MAV médullaires diagnostiquées la même période, représentant 68% des malformations artérioveineuses rachidiennes traitées au sein du service. Tous nos patients sont de sexe masculin. L’âge moyen est de 50 ans avec des extrêmes entre 37 et 65 ans. Au moment du diagnostique tous nos patients avaient un déficit moteur qui allait d’une discrète paraparésie permettant la marche (cas n°1, 2, 9) à une paraplégie complète confinant le malade à la chaise roulante (cas n°2). Tous les malades présentaient une hypertonie spastique, avec syndrome pyramidal dans trois cas (n°1, 2 et 5). Les troubles sensitifs étaient inconstants à type de paresthésies dans 2 cas (n° 1 et 2), anesthésie en selle dans un cas (n°1) et hypoesthésie à niveau sous ombilical dans un cas (n°2). Concernant les résultats des explorations radiologiques (Tableau 2):
Dans deux cas les patients ont bénéficié de deux examens IRM, la première exploration étant jugée insuffisante par le médecin traitant. (N°1 et 2) Dans dix cas une FAVDPM a pu être visualisée, dans un cas il s’agissait d’une fistule thrombosée (n°6). Les niveaux intéressés allaient de D4 à L4. Dans 6 cas la fistule siégeait à gauche, et dans 3 cas à droite. Le drainage veineux se faisait de façon variable, uniquement ascendante dans un cas (n°3) ou associée à un drainage descendant dans le reste des cas. La prise en charge a été chirurgicale dans 9 cas, avec abord direct de la fistule et exclusion de la veine de drainage. Dans un cas (n°11) une embolisation par un matériel particulaire a été tentée avec bonne évolution initiale mais récidive de la symptomatologie au bout de six mois, signant une réperméabilisation, le malade a été repris chirurgicalement. Les suites opératoires ont été dans tous les cas simples, il ne fut pas noté de cas d’aggravation après chirurgie. L’évolution post-opératoire a été marquée par une amélioration de la symptomatologie clinique portant essentiellement sur les troubles moteurs (cas n°3, 4, 7, 8, 9 et 11), une simple stabilisation des lésions dans le cas n°1. La surveillance radiologique post opératoire a consisté en une artériographie de contrôle montrant l’exclusion de la fistule, une IRM médullaire à 6 mois dans 2 cas (n°4 et 11) montrant la disparition des anomalies IRM. Le recul moyen est de 2 ans. DISCUSSION Les fistules durales rachidiennes se définissent comme un shunt artèrioveineux microscopique de 40 à 140μ (10), situé en extra-médullaire, dans l’épaisseur même de la dure-mère. Il s’agit d’une communication directe entre une ou plusieurs artérioles radiculo-méningées et une veine radiculaire unique se drainant vers les veines périmédullaires. C’est un shunt à faible débit, le plus souvent situé en regard du trou de conjugaison ou sur le trajet d’une racine postérieure. Toute fistule est constamment associée à des perturbations du drainage veineux médullaire. Le drainage veineux se fait de manière descendante vers les veines de la queue de cheval ou ascendante vers la fosse cérébrale postérieure. Leur étiopathogénie reste incertaine, leur âge tardif de survenue leur fait attribuer une origine acquise (6). Leur mécanisme d’expression clinique est en rapport avec une ischémie médullaire d’origine veineuse traduction de la gêne au retour veineux accompagnant le développement de la FAVDPM (13). Les malformations vasculaires médullaires restent une pathologie rare (25). Actuellement les fistules durales sont reconnues comme étant les malformations vasculaires médullaires les plus fréquentes (18) DJINDJIAN sur une série de 296 MAVs médullaires, retrouvait 35% de FAVDPM et BRUNERAU (5) sur une série de 140 MAVs, retrouvait 28% de FAVDPM. Dans notre série elles constituent 68%. Le tableau clinique typique associe un début fruste avec un délai diagnostique souvent supérieur à 1 an comme dans notre série (24-22). Il constitue un tableau de myélopathie progressive associant des troubles moteurs intéressant les membres inférieures le plus souvent, troubles accompagnés de troubles sensitifs et sphinctériens. Cette symptomatologie est souvent asymétrique aggravée par l’effort et la manuvre de Valsalva (14). Non traité il évolue vers une paraplégie définitive. Des cas d’aggravation aigue ont été rapportés (22). Leur Topographie est essentiellement dorsale et dorsolombaire de rares cas de localisation cervicale ou sacrée ont été rapportée (15- 20). Apport de la radiologie L’IRM médullaire est l’examen à réaliser en première intention devant toute suspicion de FAVDPM. (Figure 1) L’examen doit comporter une exploration dans les trois plans et comporter une injection de Gadolinium. La fistule elle-même n’est pas visible étant de taille microscopique, l’IRM permet de montrer les signes de présemption qui sont :
Les séquences plus récentes d’angioIRM médullaires permettraient d’affiner cette analyse radiologique (3) en orientant vers le niveau de la fistule préparant ainsi l’angiographie qui reste le seul examen permettant d’affirmer de manière certaine le diagnostique et le siège de la FAVDPM. L’exploration angiographique doit comporter l’opacification de toutes les branches radiculomédullaire, l’alimentation de la fistule pouvant être multiétagée (23). Elle doit également identifier la naissance de l’ASA. Elle permet de visualiser le shunt, les pédicules nourriciers et les veines de drainage qui sont essentiellement postérieures. Le shunt est de très petite taille. Il est indiqué par un brutal changement de calibre entre l’artère nourricière et la veine de drainage. Il se projette habituellement, sur l’incidence de face, en dessous ou en dedans du pédicule vertébral. Un signe diagnostique spécifique serait le retard du retour veineux de l’ASA de l’ordre de 15 à 20 secondes (4). Le diagnostique différentiel se pose sur le plan clinique avec une compression médullaire lente et toutes les causes de syndrome de la queue de cheval et de radiculalgie lombaire. Le but du traitement est d’exclure définitivement le shunt artérioveineux pour permettre la normalisation de la pression dans le réseau veineux périmédullaire. Comme dans notre série le traitement chirurgical est simple (1) et permet la guérison dans la majorité des cas (19). Le traitement endovasculaire comporte un risque d’aggravation neurologique et de reperméabilisation comme dans notre cas n° 7. Une de ses contre indications est la naissance de la fistule à partir d’une des branches de l’ASA. (8) Le pronostic reste lié essentiellement à la durée d’évolution des signes cliques (17) malheureusement sous nos contrées le fait que cette pathologie reste encore méconnue ajouté à la faible disponibilité des examens IRM et explorations neuroradiologiques invasives ont tendance à allonger le délai diagnostic. CONCLUSION Les FAVDPM sont une pathologie rare mais invalidante. Elles sont accessibles à un traitement curatif d’autant plus efficace que le diagnostique est porté précocement. Toute myélopathie progressive chez un patient de plus de 40 ans doit faire évoquer le diagnostique et conduire à la réalisation rapide d’une IRM médullaire complétée d’une artériographie médullaire pour le diagnostic de certitude. Ceci permettra un traitement dans les meilleurs délais. Tableau n° 1 : Résumé des données cliniques
Tabeau N°2 : Résumé des données radiologiques.
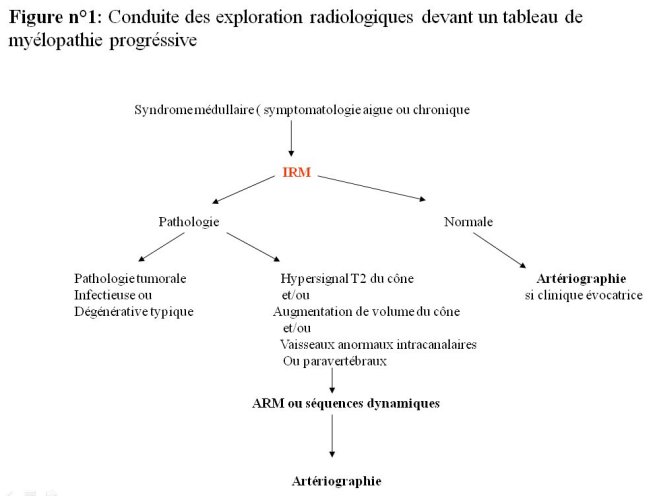 Figure 1 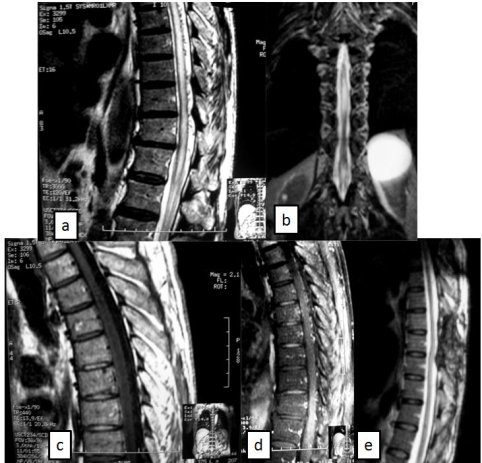 Figure 2 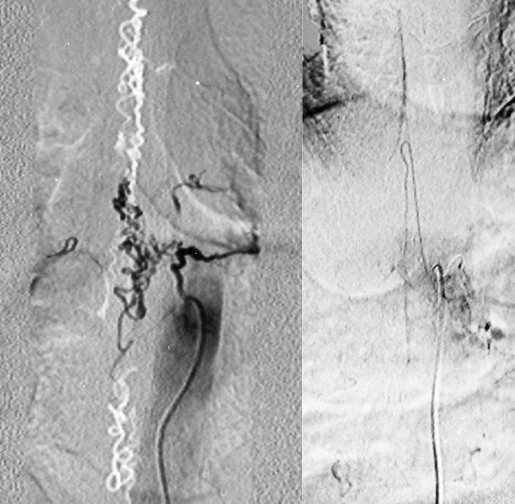 Figure 3 REFERENCES
|
© 2002-2018 African Journal of Neurological Sciences.
All rights reserved. Terms of use.
Tous droits réservés. Termes d'Utilisation.
ISSN: 1992-2647