EDUCATION / ENSEIGNEMENT
L’HEMATOME EXTRA-DURAL
EXTRA DURAL HEMATOMA
- Service de Neurochirurgie, CHU NORD Université de la Méditerranée MARSEILLE
DEFINITION
L’hématome extra-dural (HED) ou épidural est une collection sanguine développée entre la dure-mère et l’os du crâne. Les transports médicalisés et les scanners cérébraux ont beaucoup contribué à la rapidité du diagnostic et donc à la qualité du traitement de ces blessés. L’HED représente toujours une grande urgence neuro-traumatologique. Il ne faut plus hésiter à l’heure actuelle à transférer pour un scanner un traumatisé crânien même minime, car c’est à ce prix que l’on tendra vers une mortalité nulle et à une guérison sans séquelle de l’ H.E.D. pur
L’évolution en quelques heures vers des lésions cérébrales irréversibles et la mort impose une intervention en extrême urgence dès l’apparition des premiers signes cliniques.
Cette intervention devra être réalisée dans le service d’accueil primaire si le délai d’évacuation dans un centre de neurochirurgie dépasse deux heures. Notre expérience repose sur 125 cas observés de 1995 à 2000.
Les aspects modernes de la question relèvent des progrès de l’imagerie en ce qui concerne notamment l’exploration des cas asymptomatiques où l’indication chirurgicale peut se discuter mais aussi dans les cas de patients sédatés intubés et ventilés où le scanner permet d’établir le diagnostic alors que le classique drame en trois temps clinique échappe au clinicien . Il faut par ailleurs insister , sur le caractère évolutif des lésions intracraniennes , ce qui justifie un second examen tomodensitométrique si le premier a été réalisé dans les trois premières heures suivant l’accIdent . Cette dernière notion permet d’individualiser les H.E.D. « retardés » lorsque le premier scanner est normal .
I – DONNEES GENERALES
A – ETIOLOGIE
1 – Fréquence
Classiquement, l’HED complique 1 à 5 % des traumatismes crâniens graves hospitalisés dans les services de neuro-chirurgie. [5] et touche 9% des traumatismes sévères (G.C.S. 8 et plus). Certains centres spécialisés rapportent par contre un taux de fréquence de 20%.
De même si l’on considère les données autopsiques, la fréquence est plus importante : 20 à 25 % d’HED étant retrouvés parmi les facteurs responsables des décès secondaires à des accidents de la voie publique.
Enfin l’HED représente 20 % des interventions pour hématome ou collection intra-crânienne traumatique.
2 – Age – Sexe
L’HED de l’enfant représente le 1/3 des cas observés avec cependant des variations suivant les auteurs et suivant l’âge limite considéré, mais Il est surtout observé dans les seconde, troisiéme et quatriéme décades [5]
Chez le nourrisson, il est loin d’être exceptionnel alors qu’il est en théorie très rare au delà de 60 ans du fait de l’adhérence à cet âge de la dure-mère à la voûte du crâne. En réalité, on retrouve 10 % des cas chez les sujets de plus de 60 ans.
La prédominance du sexe masculin est classique en traumatologie.
3 – Le traumatisme
Ce sont les accidents de la circulation qui fournissent le contingent le plus important et le plus grave des blessés (2/3). Les chutes se retrouvent dans 1/3 des cas. Chez l’enfant, cette proportion est inversée.
Dans 20 à 25 % des cas, il existe une ou plusieurs lésions graves associées qui sont par ordre de fréquence :
fractures des membres,
traumatisme thoracique, abdominal, rachidien, maxillo-facial.
L’association avec une ou plusieurs autres lésions intra crâniennes telles qu’hématome sous dural aigu ou contusion cérébrale varie de 10% à 50% des cas suivant les auteurs.
B – ANATOMIE PATHOLOGIQUE
L’HED est localisé, parfois étendu.
Chez l’adulte au-delà de 65 ans, la dure-mère est moins facilement décollable ce qui rend l’HED moins fréquent et plus focalisé. Les localisations temporale et pariétale sont les plus fréquentes (70 %). En rapport avec la présence et le calibre significatif de l’artère méningée et de ses branches à ce niveau. La région temporale est la plus fréquemment atteinte (60 à 80% des cas) suivie de la région frontale (7% à 18%) viennent ensuite la base de la fosse moyenne et la fosse postérieure [12, 8]. Plus de 90% des cas présentent une fracture du crâne .
Le volume peut atteindre 300 à 400 cc, habituellement il est de 100 à 200 cc. Il s’agit de caillot organisé adhérent à la dure-mère.
1 – Le saignement
Dans 1 cas sur 3 , il existe une blessure de l’artère méningée moyenne visible à l’intervention, mais le saignement peut également provenir de l’os fracturé ou des sinus veineux [12]
Chez l’adulte, l’artère méningée moyenne chemine dans une gouttière ou un canal osseux. Un trait de fracture croisant ce trajet peut donc blesser l’artère.
Pour un motif de calibre l’HED est d’autant plus grave que l’artère est lésée au début de son trajet.
Enfin dans un certain nombre de cas, la dure-mère saigne de façon diffuse en regard du point d’impact du choc et du trait de fracture.
2 – Les lésions osseuses
La fracture est visible sur 85 % des radiographies, parfois, elle n’est visible qu’à l’intervention. Nous avons cependant qu’il existe 5 à 10 % des HED sans fracture décelable.
3 – Les lésions associées endocrâniennes
Il est fréquent (1/3 des cas) de trouver des lésions cérébrales sous-jacentes à l’HED (contusion, dilacération).
Cette notion rend compte du nombre élevé de formes cliniques « atypiques ».
C – PHYSIOPATHOLOGIE
On oppose classiquement l’HED d’origine artérielle souvent volumineux et déprimant profondément la dure-mère.se constitue généralement en quelques heures. L’artère continue à saigner jusqu’au coma terminal ce qui explique la rapidité évolutive de l’HED et son pronostic gravissime par compression aiguë rapidement progressive de l’hémisphère cérébral puis hernie de la partie interne du lobe temporal dans l’incisure de la tente du cervelet enfin écrasement du tronc cérébral au niveau des pédoncules.
La rupture des veines épidurale ou des sinus veineux provoque un hématome moins rapide dans sa constitution. L’hémostase se fait dans ce cas par équilibre entre la pression intra-crânienne cérébrale et la pression de l’hématome.
II – DIAGNOSTIC POSISTIF
Le dogme de l’HED avec intervalle lucide siégeant dans la zone décollable de Gérard Marchand survenant chez l’adulte jeune doit être révisé.
Cette forme classique est moins fréquente que la forme « atypique » car l’intervalle lucide peut manquer, l’hématome peut siéger n’importe où et survenir chez tout individu y compris le vieillard et l’enfant.
A – FORME TYPE
L’HED dans 12 à 34 % des cas se traduit par un drame en trois temps aboutissant au décès du malade en quelques heures . En général, l’évolution de la maladie se fait en moins de 48 H. Par contre 8% à 24% des patients n’ont pas d’ altération de la conscience , 23% à 44% n’ ont pas d’ intervalle de lucidité et sont
d’emblée dans le coma et .2O% à 28% présentent une perte de conscience immédiate post traumatique brève [12, 5, 8]. En pratique, il convient cependant de retenir que le schéma évolutif classique de l’H.E.D. est rare et qu’ en dépit de signes cliniques minimes , un traumatisé crânien peut présenter des lésions anatomiques sévères révélées par un scanner effectué à un stade précoce [3]
1 – Le traumatisme (premier temps)
Il est direct le plus souvent mais tout est possible. La violence du choc est des plus variables et il suffit qu’il provoque une fracture du crâne. L’hématome siège en règle générale en regard du point d’impact du traumatisme et du trait de fracture. Une brève perte de conscience de quelques secondes peut suivre immédiatement le choc comme dans la plupart des traumatismes crâniens mais elle n’a pas de signification particulière.
2 – L’intervalle libre (deuxième temps)
Intervalle de lucidité J.L. Petit.
Il dure de 6 à 24 H. Le sujet est parfaitement conscient et vaque normalement à ses occupations. Il existe souvent pendant cette période, une douleur d’aggravation progressive au point d’impact du traumatisme. A l’heure actuelle, tout traumatisé du crâne bénéficie d’une radiographie ou/et d’un scanner cérébral et si ce dernier examen est réalisé rapidement, il peut mettre en évidence dès ce stade précoce, un trait de fracture qui incitera à la surveillance la plus rigoureuse même s’il n’y a pas d’hématome . A la moindre aggravation clinique ce TDM doit être refait. Les cas opérés avant 48 heures représentent 75% des cas [ 20, 10 ]
3 – L’aggravation secondaire (troisième temps)
A partir de ce moment là, chaque minute compte, à tout instant, le patient peut sombrer dans un coma irréversible. La survie dépend de la rapidité de l’intervention. Il se constitue un double syndrome d’hypertension intra-crânienne aiguë associée à des signes de focalisation neurologique. Ces deux syndromes s’aggravent simultanément très rapidement et peuvent conduire au coma irréversible et à la mort en quelques minutes ou quelques heures. Les signes de souffrance axiale sont le fait de patients arrivés tardivement en salle d’ opération ou présentant des lésions intracrâniennes associées ; le pronostic dans ces cas est alors mauvais avec une mortalité pouvant atteindre 77% [8, 6] .
l’Hypertension intra-crânienne aiguë :
. les céphalées d’abord localisées deviennent diffuses, pulsatiles, accompagnées par un état nauséeux avec vomissements . Apparaît parallèlement une torpeur progressive ou au contraire un état d’agitation et, peu à peu le patient sombre dans le coma. Dès ce moment peuvent exister des manifestations végétatives et une bradycardie avec pouls tendu, ralenti de ¼ H e, ¼ h, 60…50…40 qui traduisent une compression aigüe et rapide des structures végétatives du tronc cérébral..
Les signe de focalisation :
localement : il existe une douleur à la pression d’une fosse temporale. Même obnubilé, le blessé réagit à la pression de la tempe au niveau de la mastoïde au niveau de laquelle l’une ecchymose signe une fracture temporale.
. l’examen neurologique : si l’état de conscience est encore bon, l’hémiparésie contro-latérale est facile à mettre en évidence. Si le coma est déjà installé, il faudra rechercher le déficit moteur par une asymétrie des réflexes de défense, une chute plus rapide en extension. De même, des troubles phasiques ou une altération du champ visuel ne peuvent être mis en évidence que chez un sujet encore conscient.
. l’examen oculaire : il est également capital. Au début, il existe une asymétrie puis une dilatation pupillaire unilatérale avec une arélfexie siégeant du côté de l’hématome (mydriase). Elle traduit le plus souvent l’engagement du lobe temporal, signe d’une extrême gravité qu’il ne faut pas attendre pour poser la diagnostic .
Ces signes de focalisation n’ont de sens que s’ils sont secondaires, il se distinguent ainsi de ceux qui sont apparus immédiatement après le choc et qui relèvent alors de la lésions cérébrales associées.
La détérioration clinique est alors très rapide. Le niveau de conscience s’altère en quelques minutes. Les signes de focalisation neurologique deviennent évidents (déficit moteur contro-létarl, mydriase homo-latérale à l’hématome).
Des troubles végétatifs apparaissent alors signant l’installation d’un état rapidement irréversible et traduisant l’engagement central :
troubles du rythme et de la fréquence respiratoire,
crises de décérébration uni-latérale puis bilatérale,
mydriase d’abord uni-latérale puis bilatérale.
En l’absence de réanimation intensive, le décès est inéluctable.
La mortalité et la morbidité sont directement liées au niveau de conscience au moment de l’acte chirurgical . Il est donc capital de détecter un hématome épidural avant la détérioration clinique, l’apparition de troubles de la conscience et des signes de focalisation [10] . Lobato [10] a établi une classification tomodensitométrique des lésions traumatiques intra crâniennes en corrélation avec le pronostic vital et fonctionnel : dans les formes pures d’H.E.D. , la guerison sans sequelle survient dans 84% des cas .
B – FORME PARTICULIERE
Elles sont plus fréquentes que la forme classique type et représentent 60 % des cas opérés.
1 – Formes évolutives
Elles ont été individualisées par Fénelon (1965) , classification reprise par Vigouroux (1982) [18]
L’utilisation de la tomographie axiale (scanner) en neuro-traumatologie d’urgence et l’organisation des SAMU permettent à l’heure actuelle d’intervenir de façon de plus en plus efficace dans les cas les plus dramatiques.
Formes aigues :se constituants dans les 24 premières heures
Elles représentent dans les statistiques les plus récentes plus de la moitié des cas.
Ce sont :
des blessés admis dans le coma survenu immédiatement après le traumatisme crânien, et se détériorant rapidement avec ou sans signe de focalisation. Il existe dans la plupart de ces cas des lésions associées .
des cas dont l’aggravation secondaire s’est faite très brutalement en moins de 6 H .
L’hématome est alors d’origine artérielle et il existe souvent des lésions cérébrales associées penchymateuses. La mortalité globale y est de ce fait très élevée (2/3 des cas).
Formes sub-aigues : 20 %
L’aggravation secondaire se produit entre la 24ème heure et le 7ème jour.
Le saignement est alors osseux ou veineux. Le tableau clinique est très évocateur. Le pronostic est bon. La crainte de ces cas justifie l’hospitalisation d’une semaine des traumatisés crâniens avec fracture et la réalisation d’ un second scanner au moindre doute .
Formes chroniques : 5 %
Les signes neurologiques se constituent au-delà du 7ème jour. La topographie habituelle est frontale ou occipitale. Cette dernière forme serait liée à un saignement d’ origine veineuse .
Formes asymptomatiques :
Elles sont de plus en plus fréquentes. Le diagnostic est posé lors d’un examen systématique au scanner chez un traumatisé avec fracture, alors qu’il n’existe aucun signe neurologique d’appel. Cette attitude ne peut être systématique pour tous les blessés du crâne, mais l’intervention permet dans ces cas de traiter les blessés avant l’apparition de tous signe cliniques.
– Formes « retardées » : il s’ agit de cas constatés plus souvent actuellement depuis la généralisation des transports rapides , du scanner systématique répété à distance de l’accident. La définition d’ un H.E.D. retardé est faite essentiellement sur la base de la tomodensitométrie .Il s’agit d’ une lésion non visible sur le premier C.T.scan.post traumatique mais qui le devient sur l’examen suivant . L’absence de fracture visible ne doit pas faire exclure l’éventualité du développement d’un H.E.D.retardé . Cette lésion est peu fréquente chez l’enfant, alors que chez l’adulte , elle représente entre 5% et 10% des H.E.D. La lésion peut apparaître quelques heures après l’accident et jusqu’à 16 jours après le traumatisme. La persistance de céphalées violentes doit dans ce cas conduire à réaliser le C.T. scan diagnostic. En pratique ,il faut retenir que chez le patient rapidement prise en charge le moindre doute doit conduire à pratiquer un second C.T. scan.
2 – Formes topographiques
les hématomes « des extrêmes » : Ce sont les hématomes frontaux ou les hématomes occipitaux. Ce sont des hématomes polaires, se développant en zone peu parlante, évoluant sur un mode sub-aigu ou même chronique. L’aggravation brutale avec engagement temporal ou cérébelleux peut survenir à tout instant et justifie donc de les considérer comme des cas particulièrement urgents à traiter.
les hématomes du vertex doivent être rapprochés à ces cas. Ils sont dus à une blessure longitudinal supérieur.
Les hématomes « temporaux » : ils peuvent revêtir deux formes classiques qui sont en général difficiles à individualiser dans les statistiques mais sont facilement reconnaissables au lplan chirurgical.
les hématome latéraux : ils se collectent en regard de l’écaille temporale et diffusent vers le haut et l’arrière dans la classique zone décollable de Gérard Marchand. Ils correspondent à la description classique type de l’HED . La région temporale est intéressée dans plus de la moitié des cas ( temporaux 12% , temporo-parietaux 27%, fronto-temporo-parietaux 12% ) [6].
les hématome sous-temporaux correspondent aux formes sur-aigues : La fracture se situe à la base du crâne avec blessure de l’artère méningée moyenne dans sa portion la plus volumineuse au niveau du trou petit rond. L’hématome soulève le lobe temporal et peut même donner par lui-même des signes de compression pédonculaire directe (forme sphénotemporale de Duret ). Il peut également diffuser vers l’écaille occipitale et s’étendre de façon importante vers le centre de l’hémisphère ou vers la loge cérébelleuse.
les hématomes de la fosse postérieure : la lésion est soit d’origine veineuse soit d’origine artérielle
( cf.chapitre .particulier).
Il faut souligner enfin l’ existence de formes bilatérales ( 3 à 6%) et multiples (7%) dont le diagnostic est devenu plus aisé depuis le scanner [6] .
3 – Formes étiologiques
Chez le jeune enfant, un tableau d’anémie aiguë avec pâleur associé aux signes cliniques habituels peut être un argument de poids pour poser le diagnostic. Cette anémie n’est pas présente chez l’adulte. Par ailleurs l’intervalle libre est court et la fracture du crâne est souvent mal visible.
C – EXAMEN COMPLEMENTAIRES
En pratique le diagnostic d’HED reste cliniquement difficile en urgence et sauf dans la forme la plus typique, rien ne permet d’en affirmer avec certitude la diagnostic en regard des autres complications des traumatismes crâniens. L’amélioration des transports, la médicalisation immédiate des blessés, la diffusion des scanners ont permis une indiscutable amélioration du diagnostic et du traitement.
1 – Tomographie computérisée (scanner)
C’est le seul examen permettant en urgence de faire un bilan lésionnel et un diagnostic topographique. Typiquement, l’HED se présente sous forme d’une lentille bi-convexe bien limitée d’hyperdensité élevée et donc l’angle de raccordement avec la voûte du crâne est toujours obtu. La fracture est rarement visible sur les coupes mais un hématome du scalp est pratiquement constant en regard de l’HED.
Les associations pathologiques sont fréquentes (50 % des cas) : contusion sous-jacente et diamétralement opposée, parfois bi ou plurifocales. Les signes indirects doivent être précisés : déviation des ventricules, engagement cingulaire ou temporal avec comblement des citernes.
2 – Radiographies du crâne
Tout traumatisme crânien devait comporter quatre clichés radiographiques :
Deux radios de profil,
une face nez-front sur plaque,
-un face occiput sur plaque (Worms-Bretton)
L’intéret des examens radiographiques crâniens systématiques peut est discuté et ne revêt que peu d’importance par rapport à la TDM dont l’apport en terme de bilan lésionnel bien supérieur.
En cas d’HED, la fracture est visible dans 90 % des cas. Des clichés normaux ne permettent pas d’éliminer le diagnostic, la fracture n’étant visible qu’à l’intervention. Certains hématomes d’origine veineuse peuvent d’autre par évoluer sans fracture.
Dans des cas très rares une simple radiographie du crâne révélant une glande pinéale calcifiée déviée peut emporter la décision.
3 – Angiographie cérébrale
Son intérêt a diminué depuis l’apparition du scanner. L’aspect clinique typique est celui d’une lentille bi-convexe avasculaire, correspondant au décollement des vaisseaux corticaux. Parfois on voit une flaque de produit de contraste au niveau de la plaie de l’artère méningée (signe de Lindgren). Un ralentissement circulatoire associé traduit des lésions parenchymateuses de mauvais pronostic.
4 – Autres examens
EEG : son intérêt est limité en urgence. Il peut être un des éléments de dépistage d’une forme sub-aigue ou chronique.
F.O : une stase papillaire ne se rencontre que dans les phases chroniques.
Echographie : elle est peu utilisée et montre un déplacement de la ligne médiane.
III – DIAGNOSTIC DIFFERENTIEL
A – L’HED typique et caractéristique
La grande cause d’erreur est la contusion cérébrale post-traumatique (bleu du cerveau). Il existe alors un intervalle libre pouvant aller jusqu’à 48 H, des signes de focalisation puis des signes neuro-végétatifs. La fracture du crâne est rare. Cette forme de contusion cérébrale en l’absence de scanner ou d’artériographie doit conduire à la réalisation de trou de trépan explorateur.
L’hématome intra-cérébral aigu de même que l’hématome sous-dural aigu précoce, peuvent également conduire à l’intervention et cela d’autant que l’aspect clinique correspond habituellement à celui d’un HED aigu avec coma très précoce et aggravation progressive.
B – Dans les formes les plus atypiques
Le diagnostic devient alors cliniquement impossible. La progressivité du coma, l’aggravation des signes focaux, la situation du trait de fracture constituent des indices, mais seul un trou de trépano-exploration donne la certitude en l’absence de scanner pratiqué en urgence.
En pratique, la question du diagnostic différentiel se pose uniquement dans les cas où l’on ne dispose pas de scanner, où l’évacuation du patient dure plusieurs heures et où le malade s’aggrave rapidement.
Il faut alors réaliser une trépano-ponction car l’HED doit rester une obsession en raison de sa survenue imprévisible et de son risque vital en l’absence d’évacuation urgente.
IV – TRAITEMENT
A – METHODES THERAPEUTIQUES
Dès le diagnostic d’HED posé, une décompression cérébrale rapide est impérative a comparé deux séries d’ H.E.D. et passe d’une mortalité de 33% à 8,9% lorsque les blessés ont été adressés directement du lieu de l’ accident au service de neurochirurgie le plus proche . Il décrit un délai moyen « fatal »dont la durée maximale est de 15 heures et un delai moyen « récupération sans séquelle » qui ne doit pas dépasser 2 heures .
1 – Le geste idéal
(Diagnostic certain en milieu expérimenté). Taille d’un volet crânien circonscrivant l’hématome, évacuation de cet hématome, hémostase des vaisseaux qui saignent, suspension de la dure-mère … ouverture de la dure-mère vérifiant l’espace sous-dural et l’état du cerveau sous-jacent.
Fermeture des plans superficiels avec ou sans drainage aspiratif des cavités.
2 – Le geste salvateur
(le malade s’aggrave rapidement, le délai de transport d’un centre avec scanner et neuro-chirurgie dépasse deux heures).
Dans ce cas comme le dit R. Houdart « Lorsqu’il existe une aggravation évidente et rapide, aucune temporisation ne peut être acceptable » et trois trous de trépan explorateurs doivent être réalisés:
– frontal,
temporal,
pariéto-occipital.
Si un HED est constaté, on agrandit le trou à la pince gouge de façon à évacuer les caillots et à réaliser l’hémostase du vaisseau qui saigne.
3 – Cas particuliers
Les HED de la fosse postérieure nécessitent une crâniectomie occipitale à os perdu.
Les HED du vertex doivent être évacués par un volet dépassant la ligne médiane et présentent le danger d’une blessure du sinus longitudinal supérieur.
Il faut enfin insister sur le fait qu’avant le scanner la moitié des HED échappaient au trou de trépan explorateur. C’est dire l’impérieuse nécessité de l’équipement en scanners disponibles en urgence 24h sur 24 des centre hospitaliers recevant les traumatisés du crâne.
B – INDICATIONS
Devant le diagnostic d’HED, il n’y a pas de discussion opératoire. Le degré d’urgence à retenir est d’autant plus grand que l’intervalle libre est plus court. Dés le diagnostic posé ,l’intervention doit être réalisée d’autant plus rapidement qu’il existe une inégalité pupillaire. Au delà d’un délai de 70 minutes après l’apparition de cette inégalité le risque de décès augmente de façon significative [4]
Dans les formes aiguës et dans les formes classiques, la seule possibilité de sauver le blessé est l’intervention immédiate . Autrefois avant le scanner il était possible d’envisager l’évacuation de l’hématome dans un centre primaire dans tous les cas où la durée de transport excédait 2 heures. De nos jours compte tenu de la multiplication des transports rapides médicalisés et donc du raccourcissement des temps de transfert, il semble préférable d’amener le blessé vers un centre neurochirurgical équipé où il pourra être opéré par une équipe rompue à cette technique .
Dans les formes moins dramatiques, il faut évidemment transférer le blessé dans un centre spécialisé mais à trois conditions :
au moment de la décision le malade doit être médicalisé .
le transfert doit être très rapide (inférieur à 3 heures après le diagnostic),
le service de réception doit être averti de l’arrivée du blessé et de son état.
Lobato [10] a insisté sur la mortalité supérieure des patients opérés dans le coma mais également en état de mydriase . Une détection précoce de l’hématome ainsi qu’une chirurgie en urgence sont d’une importance primordiale . Il est évident qu’ il faut opérer l’ H.E.D. dans l’ intervalle lucide comme cela a été démontré [2, 17] .Un G.C.S. bas et l’association à une contusion cérébrale assombrissent le pronostic [9]
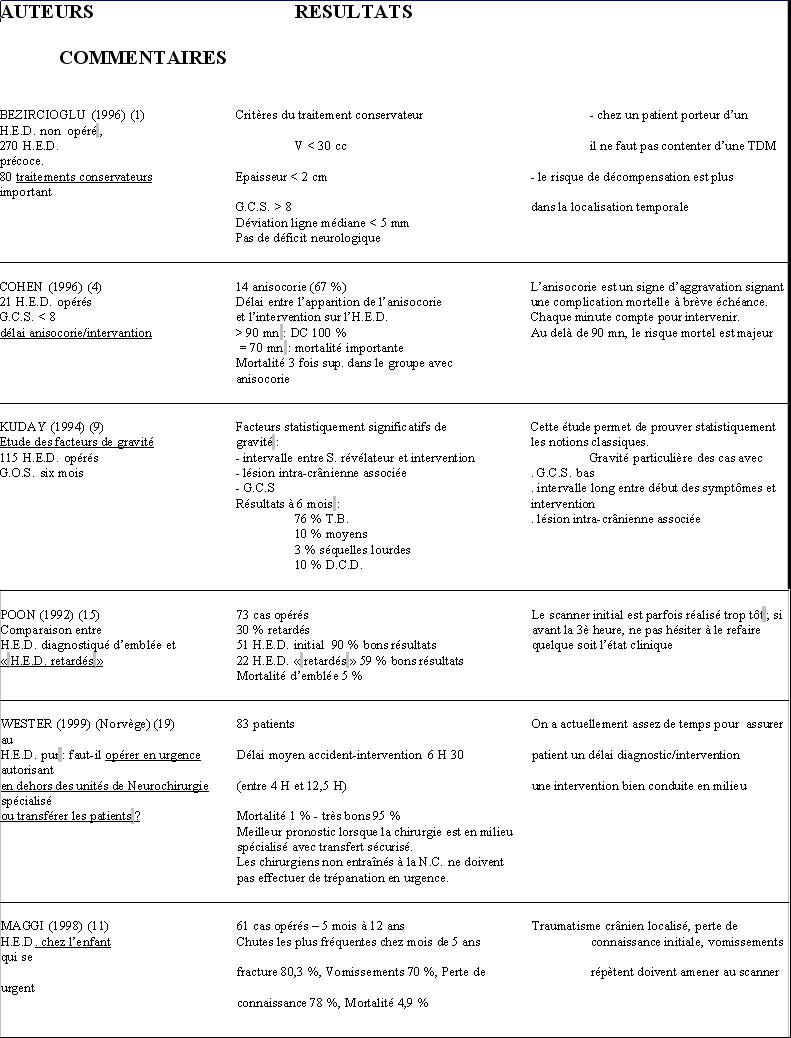
Des publications nombreuses ont argumenté sur la résolution spontanée des hématomes épiduraux post traumatiques. Le temps nécessaire à cette résorption est de 13 jours ou plus et pendant cette période ,la collection peut augmenter de volume. Des auteurs insistent sur les échecs de l’abstention chirurgicale [16]. La majorité des cas d’ H.E.D. traités avec succés sans chirurgie comportent un volume sanguin qui ne dépasse pas 40 cc. Les malades dont l’HED comporte une zone hypodense à l’intérieur d’une hyperdensité au scanner doivent faire craindre une évolution vers l’augmentation de volume et, sauf exception, doivent être opérés. Un hématome épidural peut encore augmenter de volume au delà de six à huit heure après l’ accident [13, 16] . Les cas non opérés sont traités en milieu hospitalier neurochirurgical avec possibilité de scanner et éventuellement d’ intervention immédiate .La prudence s’ impose devant les conclusions de certains auteurs estimant que l’on peut être conservateur si l’ H.E.D. est de moins de 30 cc, de mois de 20mm d’ épaisseur et dont le déplacement de la ligne médiane est inférieur à 5 mm [1]. Le risque de décompensation reste majeur , en particulier dans les localisations temporales [1] ; un hématome peut être « retardé » avec une incidence de 6 à 30%.
C – RESULTATS
1 – Mortalité
La mortalité globale des cas opérés est de 16 à 40 %. Il faut cependant distinguer les cas purs dont la mortalité est de 6 à 20 %, et les cas avec lésion cérébrale sous jacente dont la mortalité atteint 45 à 90 % suivant les statistiques . Globalement ,la mortalité doit être inférieure à 15% , y compris pour la fosse postérieure ;une plaie d’un sinus dure mérien peut augmenter ce chiffre jusqu’à 40%.
La mortalité et la morbidité restent importantes trop souvent en rapport avec un diagnostic ou des délais de transfert trop longs. Si les malades s’aggravent après l’intervention ou si l’état reste stationnaire alors qu’on attendait une amélioration, un scanner doit être à nouveau réalisé. Il montrera soit une lésion cérébrale associée mieux visible (dème, contusion hématique), soit plus rarement une récidive ou un second hématome. La mortalité globale a grandement bénéficié des progrès de l’ imagerie et de la prise en charge précoce (50% entre 1970 et 1977 ; 12,5% entre 1983 et 1984) [6].
2 – Séquelles
Elles sont très variables suivant la topographie de l’hématome et suivant l’intensité des symptômes du début. Elles sont nulles dans 50 % des cas, mineures dans 30 % et sévères dans 20 % mais dans presque tous les cas, malgré un résultat « neurologique » souvent satisfaisant, la réinsertion familiale, sociale et professionnelle n’est pas sans problème.
CONCLUSION
Au total ,on pourrait presque opposer les conclusions faites par Guillermain et Gomez dans le Livre Jubilaire du Professeur Paillas en 1979 à celles que nous pouvons établir actuellement :
le dépistage précoce de l’HED ne devrait plus être un problème à l’heure du scanner bien indiqué,
sytématique et répété en traumatologie crânienne d’urgence. Malgré l’importance de l’imagerie, la clinique reste essentielle comme facteur de prise en charge et de décision thérapeutique.
– Cette pathologie est celle qui a le plus bénéficié de la qualité et de la rapidité des transports
médicalisés à tel point qu’il devient discutable de confier le traitement chirurgical des patients à des équipes moins expérimentées dans les centres non équipés de services de neurochirurgie.
Les facteurs péjoratifs demeurent les mêmes que dans les autres lésions traumatiques crâniennes : troubles de la conscience, lésions associées, polytraumatismes, et n’ont pas varié malgré l’apport des techniques modernes de surveillance.
Les hématomes qui justifient une abstention chirurgicale doivent être sélectionnés sur des critères très précis et suivis en milieu chirurgical, le risque d’aggravation secondaire restant significatif.
En respectant rapidité et qualité des transports, de l’imagerie et de la prise en charge on devrait tendre dans les hématomes extra duraux sans lésion associée vers une mortalité zéro.
BIBLIOGRAPHIE
- Bezircioglu H, Ersahin Y, Demirçivi F, Yurt I, Dönertas K, Tektas S. Nonoperative treatment of acute extradural hematomas : analysis of 80 cases. J Trauma 1996 ; 41 : 696-8.
- Bricolo AP, Pasut LM. Extradural hematoma : toward zero mortality. Neurosurg, 1984 ; 14 : 8-12
- Callagher JP, Browder EJ. Extradural hematoma. Experience of 167 patients. J. Neurosurg, 1968 ; 29 : 1-12.
- Cohen JE, Montero A, Israel ZH. Prognosis and clinical relevance of anisocoria-craniotomy latency for epidural hematoma in comatose patients. J Trauma 1996 ; 41 : 120-2.
- Cordobes F, Lobato RD, Rivas JJ, et al. Observation on 82 patients with extradural hematoma. J Neurosurg 1981 ; 54 : 179-186.
- Devaux B, Roux FX, Chodkiewicz JP. L’hématome extra-dural à l’ère du S.A.M.U. et du scanner. Comparaison de deux séries du centre hospitalier Sainte-Anne. Neurochirurgie, 1986 ;32 , n°3
- Fenelon J. Contribution à l’étude des hématomes extra-duraux Thèse Médecine Bordeaux 1965 n° 119
- Jamieson KG, Yelland JD. Extradural hematoma. Report of 167 cases. J Neurosurg 1968 ; 29(1) : 13-23.
- Kuday C, Uzan M, Hanci M. Statistical analysis of the factors affecting the outcome of extradural haematomas : 115 cases. Acta Neurochir (Wien) 1994 ; 131 :203-6.
- Lobato RD, Rivas JJ, Cordobes F et al. Acute epidural hematoma : an analysis of factors influencing the outcome of patients undergoing surgery in coma. J Neurosurg, 1988 ; 68 : 48-57.
- Maggi G, Aliberti F, Petrone G, Ruggiero C. Extradural hematomas in children. J. Neurosurg. Sci 1998 Jun ; 42 (2) : 95 – 99.
- McKissock W, Taylor JC, Bloom WH, et al. Extradural haematoma. Observations on 125 cases. Lancet 1960 ; 2 : 167-172.
- McLaurin RL, Ford LE. Extradural hematomas : statistical survey of forty-seven cases. J Neurosurg 1964 ; 21 : 364-371.
- Miller JD, Tocher JL, Jones PA. Extradural heamatoma – earlier detection, better results. Brain Injury, 1988 ; 2 : 83-86
- Poon WS, Rehman SU, Poon CYF, Li AKC. Traumatic extradural hematoma of delayed onset is not a rarity. Neurosurgery 1992 ; 30 :681-6.
- Servadei F, Faccani G, Roccella P, et al. Asymptomatic extradural haematomas. Results of a multicenter study of 158 cases in minor head injury. Acta Neurochir 1989 ; 96(1-2) : 39-45.
- Stephanov S. Postoperative mortality in acute extradural haematoma. Br J Neurosurg, 1993 ; 7 : 461-463.
- Vigouroux RP. Traumatismes crânio-encéphaliques. Encycl. Med. Chir. Neurol, 1982.
- Wester K. Decompressive surgery for « pure » epidural hematomas : does neurosurgical expertise improve the outcome ? Neurosurgery 1999 Mar ; 44 (3) : 495 – 500.

