
|
|
|
CLINICAL CASE/CAS CLINIQUE
MYASTHENIE ET SARCOÏDOSE : A PROPOS D’UN CAS ET REVUE DE LA LITTERATURE
MYASTHENIA AND SARCOIDOSIS: A CASE REPORT AND LITERATURE REVIEW
E-Mail Contact - GUINHOUYA KOKOU MENSAH :
herve_guinhouya@yahoo.fr
Résumé Introduction L’association de myasthénie avec une sarcoïdose est très rare. Nous avons présenté un cas intéressant la coexistence d’une myasthénie et d’une sarcoïdose. Observation Une patiente de 29 ans ayant des antécédents de myasthénie sous traitement, a été admis à l’hôpital avec des antécédents da fatigue, toux sèche chronique et de dyspnée. L’examen pneumologique révèle une dyspnée stade 1et la TDM thoracique révèle la présence de ganglions médiastinales ; La fibroscopie bronchique avec biopsie et examen anatomo-pathologique montre la présence de la présence de granulomes épithélioïdes et giganto-cellulaires sans nécrose caséeuse confirmant la sarcoïdose. Conclusion La myasthénie associée à la sarcoïdose est rare, mais doit être évoqué devant une myasthénie grave associée à des manifestations pulmonaires. Mots-clés : Myasthenia gravis, saocoïdose, Lomé, Togo
Abstract Introduction The association of myasthenia gravis with sarcoidosis is very rare. We present an interesting case of the coexistence of myasthenia gravis and sarcoidosis. Case Report A 29‑year‑old female patient with a history of treated myasthenia gravis was admitted to the hospital with complaints of fatigue, chronic dry cough, and dyspnea. Pulmonary examination revealed stage 1 dyspnea, and thoracic CT scan showed mediastinal lymphadenopathy. Bronchoscopic biopsy with histopathological examination demonstrated epithelioid and giant cell granulomas without caseous necrosis, confirming sarcoidosis. Conclusion Myasthenia gravis associated with sarcoidosis is rare, but it should be considered when severe myasthenia is accompanied by pulmonary manifestations. Keywords: Myasthenia gravis, sarcoidosis, Lomé, Togo INTRODUCTION La myasthénie grave est une maladie auto-immune de la jonction neuromusculaire (8). Il s’agit d’une affection rare, dont la prévalence est estimée entre 45 et 142 cas pour 1 000 000 d’habitants. Elle peut survenir à tout âge, avec une nette prédominance féminine (6). Dans de rares cas, la myasthénie grave peut être associée à d’autres maladies auto-immunes telles que la thyroïdite de Hashimoto, le lupus érythémateux, la polyarthrite rhumatoïde ou le diabète juvénile (3). L’association entre la myasthénie grave et la sarcoïdose est encore plus exceptionnelle (4). Nous rapportons ici un cas illustrant cette association. OBSERVATION Monsieur XY, 29 ans, douanier de profession, a été reçu en consultation neurologique pour une vision dédoublée des objets surtout lors des contrôles de bagage sur l’écran du scanner, une modification du timbre de la voix ainsi qu’une faiblesse musculaire généralisée s’aggravant à l’effort. Cette consultation, effectuée le 29 décembre 2022, a permis de relever des épisodes rares de fausses routes ainsi qu’un ptosis en cas de fatigue extrême. L’examen clinique était normal. Le diagnostic de myasthénie grave a alors été envisagé. Un test à la prostigmine a été réalisé lors d’un épisode de fatigue associé à un ptosis, avec une régression marquée des signes. La recherche de l’anticorps anti-récepteur de l’acétylcholine (Ac anti-RACH) s’est révélée positive avec un titre de 0,8 nmol/ml (valeur normale < 0,2 nmol/ml). L’électromyogramme a montré une diminution modérée du potentiel moteur à la stimulation répétitive, de l’ordre de 9 %. Le scanner thoracique était revenu normal. Le patient a été mis sous pyridostigmine 60 mg comprimé à raison de un comprimé par 8 heures. L’évolution a été marquée par une régression des symptômes avec quelques épisodes de poussées. Trois ans plus tard, en Août 2025, le patient est revenu en consultation pour une dyspnée précédée depuis trois mois de toux sèche, résistante au traitement symptomatique ainsi qu’une fatigue survenant sans le moindre effort avec des épisodes de fièvre et de sueurs nocturnes. Une consultation pneumologique fut alors faite et permis de classer la dyspnée en stade 1 selon Sadoul. 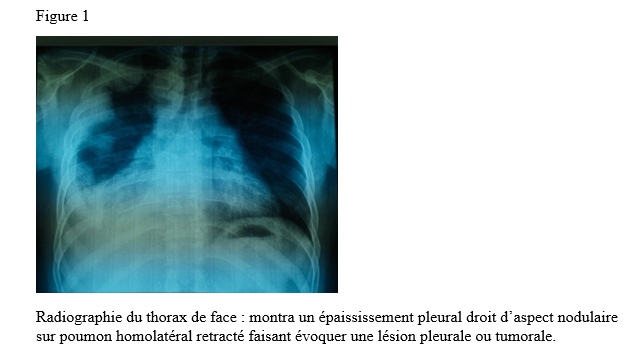 La radiographie pulmonaire de face (figure 1) montra un épaississement pleural droit d’aspect nodulaire sur poumon homolatéral retracté faisant évoquer une lésion pleurale ou tumorale. 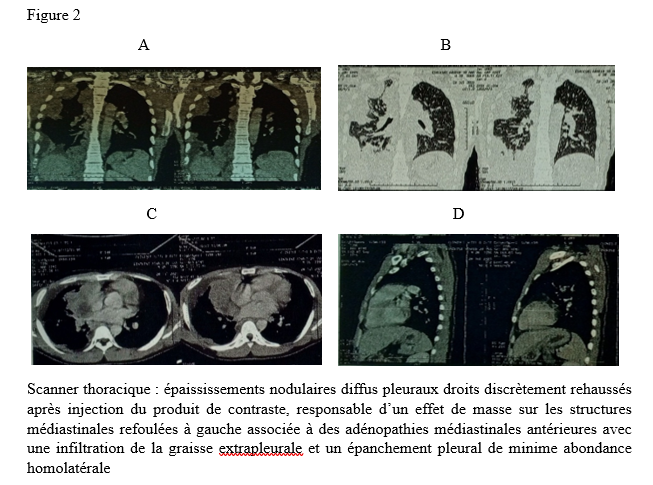 Le scanner thoracique demandé (figure 2) révéla des épaississements nodulaires diffus pleuraux droits discrètement rehaussés après injection du produit de contraste, responsable d’un effet de masse sur les structures médiastinales refoulées à gauche associée à des adénopathies médiastinales antérieures avec une infiltration de la graisse extrapleurale et un épanchement pleural de minime abondance homolatérale. Devant cet aspect scanographique, une fibroscopie bronchique fut réalisée montrant une muqueuse bronchique légèrement inflammatoire dans son ensemble avec épaississement des éperons de division entre la lobaire supérieur et moyen à droite et entre le culmen et la lingula à gauche siège de biopsie pour l’examen anatomo-pathologique sur les pièces ainsi que le genexpert du liquide broncho-alvéolaire. La recherche de tuberculose revint négative. 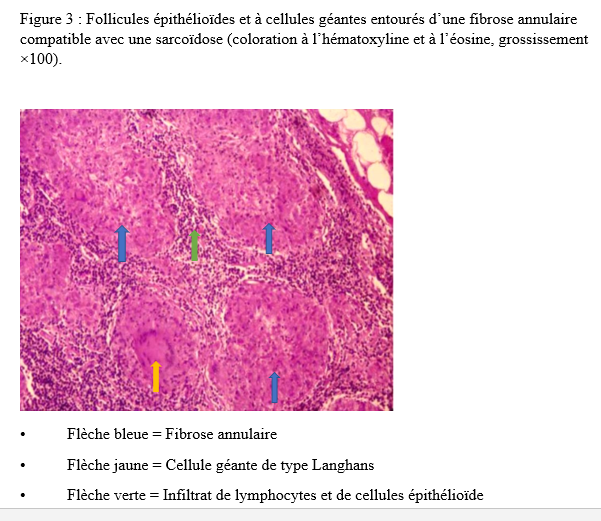 L’examen anatomo-pathologique des pièces biopsiques a permis de mettre en évidence la présence de granulomes épithélioïdes et giganto-cellulaires sans nécrose caséeuse (figure 3). L’examen de la peau et des phaners ainsi qu’une consultation ophtalmologique étaient normaux. La consultation rhumatologique était sans particularité. L’IRM cérébrale était normale. La spirométrie a révélé une CVF (FVCI) à 52 %, un VEMS (FEV1) à 63 %, VEMS/CVF> LIN avec absence de gain après bêta-2 mimétiques. Les données gazométriques étaient les suivantes : PaO₂ = 59 %, PaCO₂ = 54 %, pH = 7,39, Hb = 14,3 g/dl, HCO₃⁻ = 32 mmol/l. La calcémie était à 117mg/l ( 90-110 mg/l) l’IDR à la tuberculine est négative et le dosage de parathormone était revenu normal. Le diagnostic de sarcoïdose a été retenu chez notre patient. Un traitement par pyridostigmine 60 mg toutes les 8 heures et prednisolone à dose dégressive avec une dose d’entretien de 20 mg per os le matin au cours du repas a été instauré ainsi qu’un régime alimentaire pauvre en calcium et une exposition limitée au soleil. Ce traitement a permis une stabilisation de l’état clinique du patient sous surveillance multidisciplinaire. DISCUSSION Il est bien connu que des troubles de la réponse immunitaire peuvent coexister chez certains patients (12). Lorsque deux ou plusieurs maladies d’origine indéterminée sont retrouvées, plusieurs questions intéressantes se posent. Il est important de confirmer d’abord les diagnostics individuellement. Il est difficile d’aborder les mécanismes immunologiques qui déclenchent l’apparition de ces diagnostics ensemble. Bien que la coexistence de la MG et de la sarcoïdose puisse être une coïncidence, il convient de signaler ce cas en raison des multiples caractéristiques intéressantes observées ainsi que de la rareté de leur apparition. En effet, la survenue d’épisodes de fatigue chez un sujet myasthénique est souvent mise sur le compte d’une poussée myasthénique ce qui peut être source d’errance diagnostique. De même la survenue d’une hypercalcémie chez un sujet myasthénique peut orienter vers un trouble du métabolisme phospho-calcique en rapport avec une pathologie de la glande parathyroïde (13). Par ailleurs, la neurosarcoïdose est une complication chez 5 % des patients atteints de sarcoïdose (11). Les manifestations neurologiques les plus courantes de la sarcoïdose sont les neuropathies crâniennes dues à une méningite basale chronique. Le nerf facial est le plus souvent touché, parfois de manière bilatérale. Le nerf optique peut également être hypertrophié ou atrophié (2). L’examen ophtalmologique chez notre patient a révélé un fond d’œil normal ainsi que les nerfs oculomoteurs et il n’y avait aucun signe d’uvéite. Les autres nerfs crâniens étaient normaux aussi. L’IRM cérébrale n’a montré aucun signe de sarcoïdose. Toutes ces caractéristiques suggéraient la faible probabilité d’une neurosarcoïdose. Ainsi, l’hypercalcémie peut survenir dans les troubles formant un granulome tels que la sarcoïdose, en raison de la production rénale supplémentaire de 1,25-dihydroxyvitamine D. La libération de la PTH est inhibée par l’hypercalcémie et des niveaux élevés de calcitriol, ce qui explique la suppression du taux de PTH dans la sarcoïdose (5). Chez notre patient, le taux de PTH était normal, ce qui exclut une hyperparathyroïdie coexistante. La MG est une maladie auto-immune induite par l’apparition d’anticorps anti-acétylcholine Une dysrégulation des lymphocytes T est observée dans le sang périphérique (10). D’autre part, la sarcoïdose est une maladie systémique caractérisée par la formation de lésions granulomateuses à cellules épithélioïdes non accompagnées de nécrose, et sa pathogenèse n’est pas claire. Cependant, des informations récentes ont suggéré le mécanisme suivant de l’établissement des lésions granulomateuses des cellules épithélioïdes, bien que les détails soient encore inconnus (7). Les lymphocytes T sont activés après une stimulation non spécifique ou une stimulation en réponse immunitaire à une cause inconnue, et les lymphocytes T activés s’accumulent dans la lésion. Ces lymphocytes T accumulés produisent des lymphokines qui vont favoriser la différenciation des monocytes/macrophages en cellules épithélioïdes, ce qui entraîne la formation d’un granulome épithélioïde (7). Ceci parce que, le thymus joue un rôle important dans la différenciation et la croissance des lymphocytes T, on suppose que la MG en tant que « cause inconnue » active la lignée des lymphocytes T, induisant la formation de lésions de sarcoïdose. Toutefois, certains auteurs ont rapporté une sarcoïdose durant la période de rémission de la MG (1) d’autres une sarcoïdose pendant la période une poussée myasthénique (9) voire une régression de la MG et de la sarcoïdose après thymectomie (9). Le traitement de la myasthénie grave associée à la sarcoïdose repose en partie sur les mêmes molécules. Ainsi, notre patient a été mis sous anticholinestérasique (pyridostigmine), corticoïde (prednisolone). Nous sommes dans l’attente d’un avis spécialisé en immunologie, compétence qui fait actuellement défaut au Togo. CONCLUSION La myasthénie associée à la sarcoïdose est rare, mais doit être évoqué devant une myasthénie grave associée à des manifestations pulmonaires. Dans le contexte de la pandémie de VIH et de nouvelles pathologies émergentes en Afrique noire, il serait pertinent d’explorer systématiquement les liens possibles entre l’infection par le VIH ou des nouvelles pathologies, les infections pulmonaires associées et la survenue éventuelle de myasthénie grave associée à la sarcoïdose, afin d’optimiser la prise en charge des patients. REFERENCES 1- Andonopoulos AP, Papathanasopoulos PG, Karatza C. Sarcoïdose chez un patient atteint de myasthénie grave : étude de cas et revue de la littérature. Clin Rheumatol. 1991; 10:323-325. 2- Bradshaw MJ, Pawate S, Koth LL, Cho TA, Gelfand JM. Neurosarcoidosis: Pathophysiology, Diagnosis, and Treatment. Neurol Neuroimmunol Neuroinflamm. 2021 Oct 4;8(6):e1084. 3-Braunwald E, Fauci AS, Kasper DL, Hauser SL, Longo DL, Jameson JL. Neurologic disorders. Principles of Internal Medicine. 2001; 15:2518. 4-Diaco M, Ancarani F, Montalto M. Association of myasthenia gravis and antisynthetase Syndrome: a case report. Int J Immunopathol Pharmacol. 2004; 17(3):395-399. 5-Falk S, Kratzsch J, Paschke R, Koch C. Hypercalcémie à la suite d’une sarcoïdose avec des concentrations sériques normales de vitamine D. Med Sci Monit. 2007; 13:133-136. 6-Goulon-Goeau C, Gajdos P. Myasthénie et syndromes myasthéniques. Encycl Méd Chir, Neurologie, 17-172-B-10, 2002, 14p. 7-Izumi T. Sarcoïdose : maladie pulmonaire allergique. Nankodou Press, Tokyo, 1986; 296. 8-Lindstrom J. Experimental myasthenia gravis. J Autoimmune Neurol Neurosurg Psychiatry. 1980; 568–576. 9-Saper JR, Fry MB. Sarcoïdose se présentant sous la forme d’une masse médiastinale chez un patient atteint de myasthénie grave. Dis Nerv Syst. 1977; 38:57-59. 10-Skolnik PR, Lisak RP, Zweiman B. Analyse d’anticorps monoclonaux de sous-ensembles de lymphocytes T sanguins dans la myasthénie grave. Ann Neurol. 1982; 11:170-176. 11-Stern BJ, Krumholz A, Johns C, Scott P, Nissim J. Sarcoïdose et ses manifestations neurologiques. Arch Neurol. 1985; 42:909-917. 12-Theofilopoulos AN. L’auto-immunité. In: Stites DP, Stobo JD, Wells JV (eds). Immunologie fondamentale et clinique. Norwalk: Appleton et Lange, 1987:128-158. 13-Triggiani V, Guastamacchia E, Lolli I, Troccoli G, Resta F, Sabbà C, Ruggieri N, Tafaro E. Association d’un thymome malin largement invasif avec myasthenia gravis et hyperparathyroïdie primaire due à un adénome parathyroïdien : rapport de cas et revue de la littérature. Immunopharmacol Immunotoxicol. 2006; 28:377-85. |
© 2002-2018 African Journal of Neurological Sciences.
All rights reserved. Terms of use.
Tous droits réservés. Termes d'Utilisation.
ISSN: 1992-2647